Neuropathie is het niet goed functioneren van één of meerdere zenuwen. Ons lichaam is opgebouwd uit 3 types van zenuwsystemen namelijk het motorisch, sensibel en autonoom zenuwstelsel. Deze 3 systemen kunnen aangetast worden bij patiënten met multipel myeloom, zowel door de ziekte zelf als door de anti-myeloom behandeling. Ook kunnen een aantal speciale situaties bij myeloom patiënten de kans op neuropathie verergeren zoals het fors gebruik van alcohol, suikerziekte (diabetes), nierfalen, etc.
Motorische neuropathie (Figuur 1) omvat de aantasting van de motorische zenuwen. Motorische zenuwen hebben hun oorsprong ter hoogte van het ruggenmerg en lopen naar de vele spieren in ons lichaam. Een aantasting van deze zenuwen zal zich voornamelijk uiten onder vorm van een verlies aan kracht.

- Spierzwakte
- Afname van de spiermassa (spieratrofie)
Sensibele neuropathie (Figuur 2) is een aantasting van de gevoelszenuwen. Deze vezels brengen informatie uit de omgeving naar onze hersenen. Een aantasting van deze zenuwen uit zich door verlies van fijne tast, tintelingen, gevoel van op watten te lopen, verminderde herkenning van voorwerpen (wat verlies aan proprioceptie wordt genoemd) of door pijnen.

Symptomen
- Overgevoeligheid (hyperesthesie)
- Tintelingen/voosheid (paresthesie)
- Gestoorde gevoeligheid (dysesthesie)
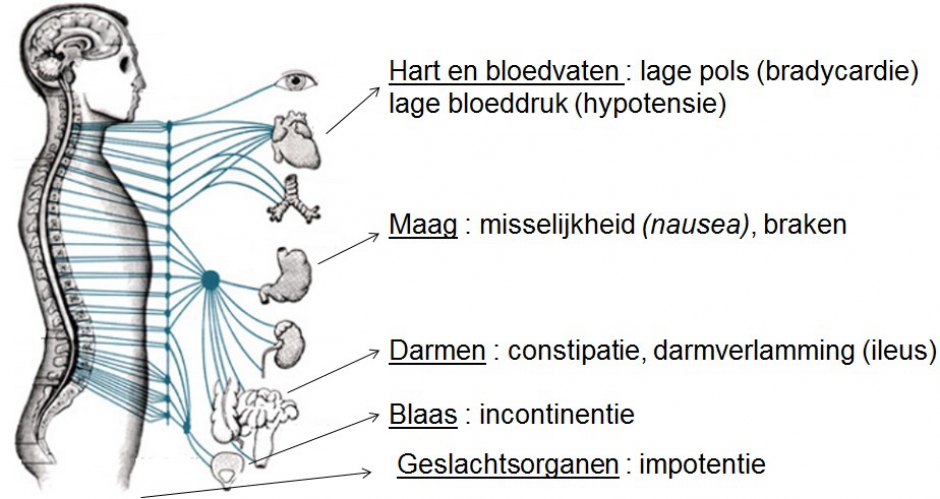
PijnHet laatste systeem dat mogelijk kan aangetast worden is het autonoom zenuwstelsel (Figuur 3). Dit zeer complex systeem regelt een aantal processen in ons lichaam waar wij geen bewuste controle over hebben. Voorbeelden zijn onder andere de zweetproductie, regeling van de bloeddruk, darmbeweging, controle over de sluitspier van de blaas, etc. Aantasting van dit systeem kan zich uiten door o.a. constipatie, bloeddrukval bij rechtkomen (wat men orthostatische hypotensie noemt), seksuele dysfunctie bij mannen, urineverlies, etc.
De diagnose van neuropathie gebeurt op basis van de bevraging van de patiënt (anamnese), lichamelijk onderzoek (o.a. testen van kracht, reflexen en gevoel door middel van een monofilament) en bijkomende technische onderzoeken. Dit laatste omvat het gebruik van de elektromyografie (EMG). Een EMG is een neurofysiologisch onderzoek waarbij door middel van fijne naalden informatie over spieractiviteit en zenuwgeleiding wordt bekomen.
De bevraging omvat het actief navragen van neuropathische symptomen. Om dit gestructureerd en volledig te kunnen laten plaatsvinden, kan een zelfbevragingstest worden gebruikt (Figuur 4).

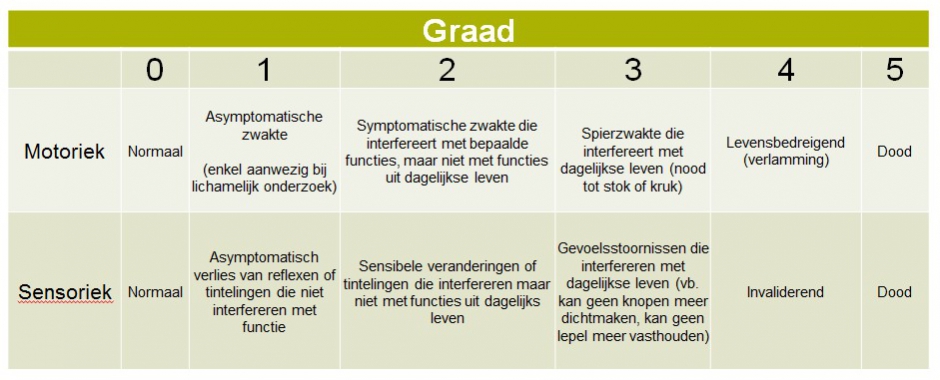
Om de ernst van polyneuropathie te kunnen kwantificeren bestaan er een aantal neuropathie schalen. De meest gebruikte neuropathieschaal is deze van het ‘National Cancer Institute’ (Figuur 5). Motorische en sensibele neuropathie worden onderverdeeld in 5 gradaties. Op basis van deze gestandaardiseerde schaal kan uw hematoloog bepaalde dosisveranderingen voor thalidomide of bortezomib doorvoeren.
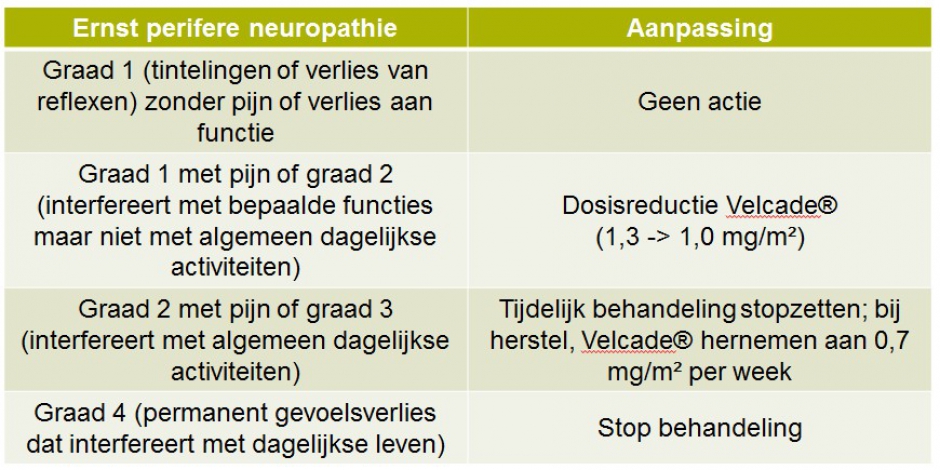
De behandeling van een neuropathie symptomen gebeurt door vermindering van de toegediende dosis of door minder frequente toediening van anti-myeloombehandelingen (Tabel 1). Soms kunnen ook geneesmiddelen of voedingssupplementen (vb. vitamines) worden toegediend die specifieke neuropathische symptomen verlichten (Tabel 2). Tot slot worden ook allerhande vormen van massage en lokale behandeling voorgesteld. Er zijn jammer genoeg weinig data beschikbaar die duidelijk het effect van deze interventies aantonen.
Tabel 2 : Farmacologische en niet-farmacologische interventies bij neuropathie
|
Farmacologische interventies bij neuropathie
Gabapentine (Neurontin ®) Start aan 300 mg – 3/d i.f.v. tolerantie à 1200 mg – 3/d Pregabaline (Lyrica ®) 150 mg p.d., geleidelijk verhogen tot 300 à 600 mg/d in 2 à 3 giften Amitryptiline (Redomex ®) Start aan 25 mg/d, verdubbel elke 2 weken (tot 100 mg/d) Duloxetine (Cymbalta ®) 20-60 mg/d Lokaal gebruik van lidocaïne/lokale verdoving
Niet farmacologische interventies bij neuropathie
Vitamine supplementen
Crèmes |
Info juli 2017 UZBrussel
Myeloompatiënten lopen een verhoogd risico op infecties. De kans op infecties is het hoogst in de eerste 2 à 3 maanden van een anti-myeloom behandeling of bij herval van de ziekte. De voornaamste infecties zijn infecties van de luchtwegen en de longen (de respiratoire infecties) en urineweginfecties (blaas- of nierinfecties).
De oorzaken voor het ontwikkelen van infecties bij myeloompatiënten zijn te vinden in een onderdrukking van het immuunsysteem. Dit systeem beschermt ons dag in dag uit tegen bacteriën, virussen en schimmels. Zowel de anti-myeloom behandeling als het myeloom zelf kunnen een aantasting van het immuunsysteem veroorzaken.
Alle myeloompatiënten hebben baat bij een jaarlijks griepvaccin (influenza) alsook pneumokokkenvaccin bij diagnose. De pneumokok is een bacterie die frequent de oorzaak is van infecties van de luchtwegen en de longen. Hoewel het vaccineren geen absolute zekerheid biedt tegen griep of pneumokokken-infecties biedt (zij vereisen namelijk een goed werkzaam immuunsysteem), zijn de vaccins veilig bij myeloompatiënten en veroorzaken zij zelden hinder.
Myeloompatiënten lopen een verhoogd risico op infecties. De kans op infecties is het hoogst in de eerste 2 à 3 maanden van een anti-myeloom behandeling of bij herval van de ziekte. De voornaamste infecties zijn infecties van de luchtwegen en de longen (de respiratoire infecties) en urineweginfecties (blaas- of nierinfecties).
De oorzaken voor het ontwikkelen van infecties bij myeloompatiënten zijn te vinden in een onderdrukking van het immuunsysteem. Dit systeem beschermt ons dag in dag uit tegen bacteriën, virussen en schimmels. Zowel de anti-myeloom behandeling als het myeloom zelf kunnen een aantasting van het immuunsysteem veroorzaken.
Alle myeloompatiënten hebben baat bij een jaarlijks griepvaccin (influenza) alsook pneumokokkenvaccin bij diagnose. De pneumokok is een bacterie die frequent de oorzaak is van infecties van de luchtwegen en de longen. Hoewel het vaccineren geen absolute zekerheid biedt tegen griep of pneumokokken-infecties biedt (zij vereisen namelijk een goed werkzaam immuunsysteem), zijn de vaccins veilig bij myeloompatiënten en veroorzaken zij zelden hinder.
Preventieve antivirale geneesmiddelen worden routinematig gebruikt bij myeloompatiënten. Patiënten behandeld met Velcade®, hoge doses corticoïden en patiënten in de zes maanden na een autologe stamceltransplantatie hebben een sterk verhoogd risico op de ontwikkeling van gordelroos (zona in de volksmond) (Figuur 11). Deze virale infectie wordt verooraakt door een heractivatie van het Herpes zoster virus en veroorzaakt een zeer pijnlijke huiduitslag die zich volgens het verloop van één zenuw bandvormig uitbreidt. Er kan ook een hersen(vlies)ontsteking ontstaan. Het toedienen van een preventieve dosis aciclovir (Zovirax®) kan de kans op deze complicaties sterk verminderen.
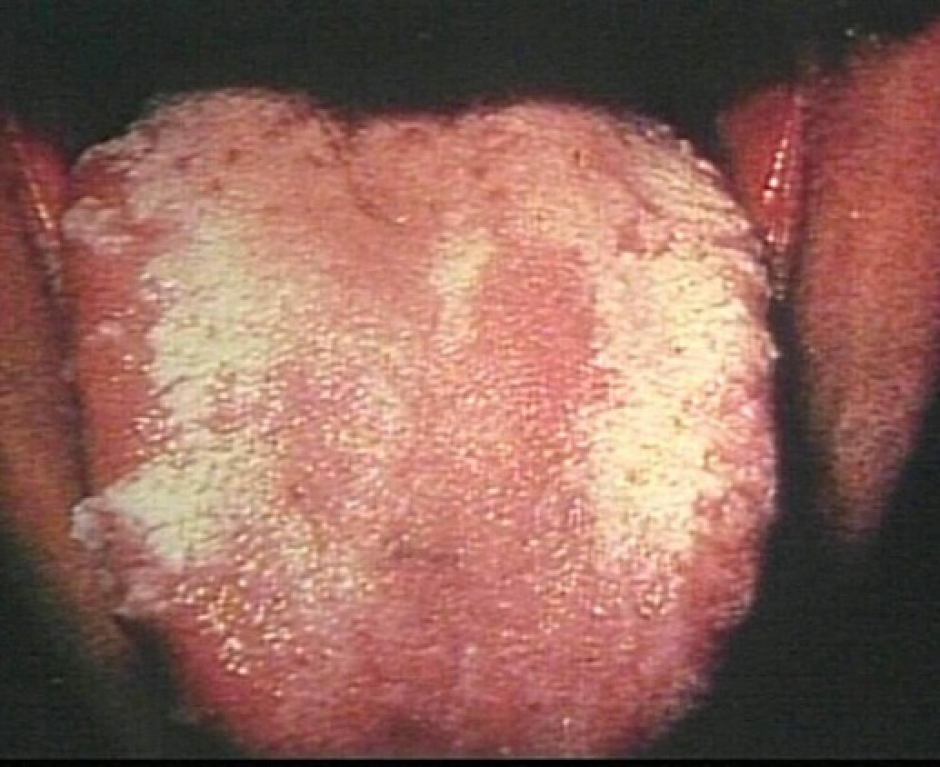
Preventieve schimmelwerende geneesmiddelen worden soms gebruikt bij patiënten die behandeld worden met hoge doses corticoïden en bij myeloom patiënten met suikerziekte. Schimmelinfecties tasten voornamelijk de mond en de slokdarm aan (Candidose) (Figuur 12). Ter preventie kan bijvoorbeeld fluconazole (Diflucan®) worden opgestart.

Preventieve antivirale geneesmiddelen worden routinematig gebruikt bij myeloompatiënten. Patiënten behandeld met Velcade®, hoge doses corticoïden en patiënten in de zes maanden na een autologe stamceltransplantatie hebben een sterk verhoogd risico op de ontwikkeling van gordelroos (zona in de volksmond) (Figuur 11). Deze virale infectie wordt verooraakt door een heractivatie van het Herpes zoster virus en veroorzaakt een zeer pijnlijke huiduitslag die zich volgens het verloop van één zenuw bandvormig uitbreidt. Er kan ook een hersen(vlies)ontsteking ontstaan. Het toedienen van een preventieve dosis aciclovir (Zovirax®) kan de kans op deze complicaties sterk verminderen.
Preventieve schimmelwerende geneesmiddelen worden soms gebruikt bij patiënten die behandeld worden met hoge doses corticoïden en bij myeloom patiënten met suikerziekte. Schimmelinfecties tasten voornamelijk de mond en de slokdarm aan (Candidose) (Figuur 12). Ter preventie kan bijvoorbeeld fluconazole (Diflucan®) worden opgestart.
Preventieve antibiotica-therapie wordt in bepaalde omstandigheden gebruikt maar is eerder uitzondering dan regel. Voornamelijk oudere patiënten en patiënten met herhaalde infecties onder zware anti-myeloom behandelingen hebben soms baat bij preventieve antibioticatherapie (vb. Ciproxine® 500 mg per dag).
Bij sommige patiënten met herhaalde bacteriële of virale infecties en een sterk verlaagde antilichaamconcentratie kan een maandelijkse intraveneuze toediening van menselijke immuunglobulines (Privigen®, Multigam®, Gammagard®, … ) soms soelaas brengen.
Infecties bij myeloompatiënten dienen snel worden behandeld met breed spectrum antibiotica. In de meeste gevallen kan dit door thuis antibiotica in te nemen maar soms moet dit tijdens een hospitalisatie gebeuren (voor intraveneuze toediening van antibiotica).
Veneuze trombo-embolie manifesteert zich voornamelijk onder de vorm van een diep veneuze trombose van het been (DVT) en/of longembolie (LE). Het risico op het ontwikkelen van een trombo-embolie is verhoogd bij myeloompatiënten; zowel door het ziekteproces zelf, als door de behandelingen die men gebruikt.
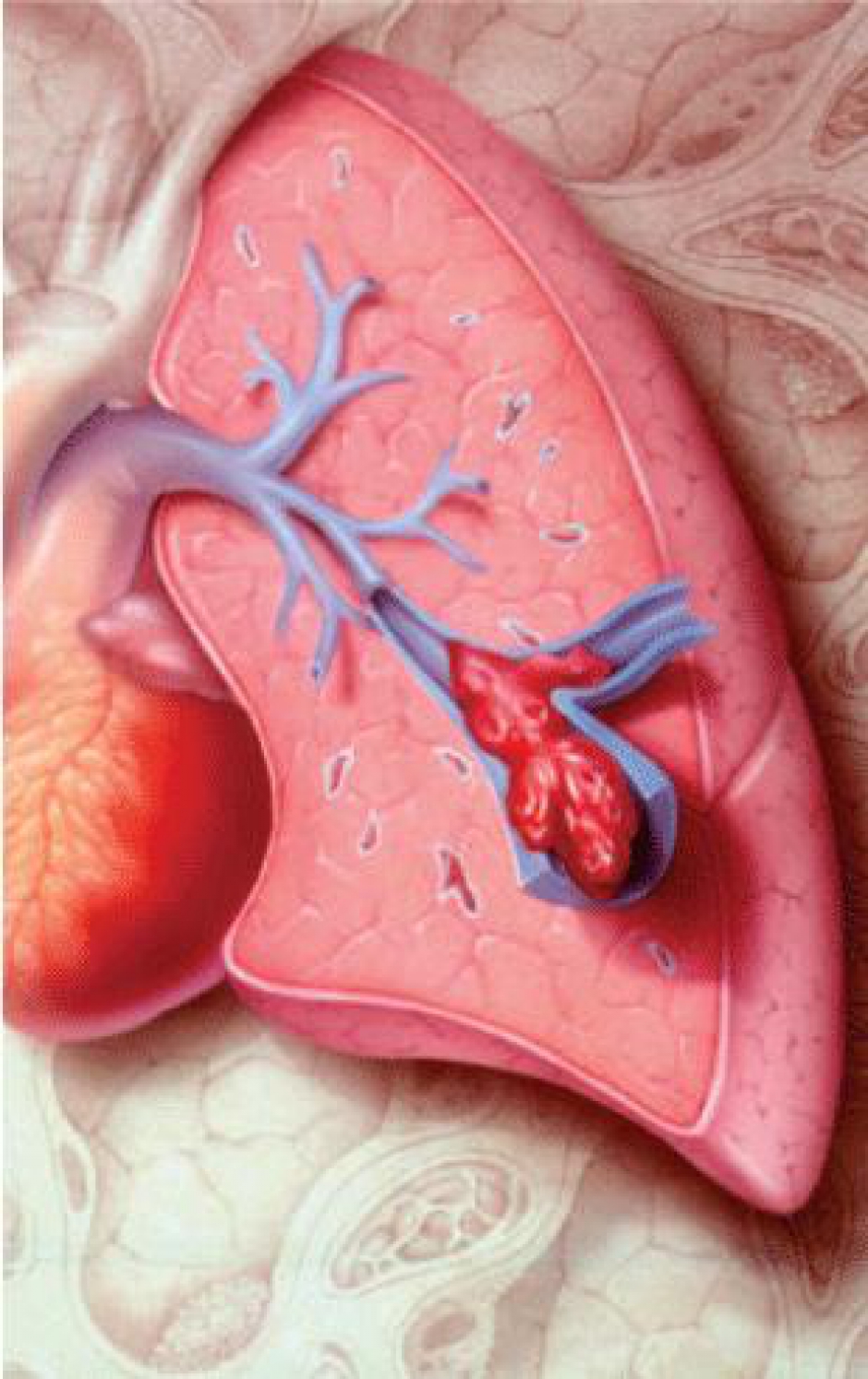
Een DVT van het been is de vorming van een bloedklonter in een diepe vene van het been (Figuur 6). Dit veroorzaakt ongemak onder de vorm van zwelling van het been, roodheid, warmte en pijn (Figuur 7). Een longembolie ontstaat meestal wanneer zo’n klonter uit één van de benen (of het bekken) loskomt (i.e. emboliseert) en met de bloedstroom terechtkomt in de bloedsomloop van de longen (Figuur 8). Dit kan zich uiten onder de vorm van pijn op de borst, kortademigheid, frequent hoesten (of ophoesten van bloed) of episodes van bewustzijnsverlies (Figuur 9). Waar een DVT een onaangename situatie met veel last is, is een LE een potentieel levensbedreigende aandoening.

Dit veroorzaakt ongemak onder de vorm van zwelling van het been, roodheid, warmte en pijn (Figuur 7).
Een longembolie ontstaat meestal wanneer zo’n klonter uit één van de benen (of het bekken) loskomt (i.e. emboliseert) en met de bloedstroom terechtkomt in de bloedsomloop van de longen (Figuur 8).


Een veneuze trombo-embolie ontstaat door een wisselwerking tussen drie factoren (Figuur 10). Enerzijds kent men de veneuze stase van bloed. Deze situatie komt voor bij myeloom patiënten wanneer zij door pijn of ziekte langdurig aan hun bed gekluisterd zijn. Anderzijds speelt ook de overmatige stolling van bloed een belangrijke rol. Deze situatie is eigen aan het multipel myeloom, voornamelijk in de maanden onmiddellijk na diagnose of tijdens combinatiebehandelingen met hoge dosissen corticoïden en thalidomide of lenalidomide. Tot slot leidt ook een beschadiging van de binnenbekleding (het zogenaamde endotheel) van bloedvaten tot een fors verhoogd risico op trombo-embolieën. Deze situatie ziet men na het gebruik van bepaalde irriterende chemotherapeutica of het gebruik van katheters. Deze drie risicofactoren werden voor het eerst beschreven in de 19e eeuw door de Duitse arts Virchow en zijn gekend als de triade van Wirchow.

Multipel myeloom patiënten lopen een fors verhoogd risico op het ontwikkelen van een veneuze trombo-embolie. Men heeft een aantal onafhankelijke risicofactoren geïdentificeerd die uw hematoloog in staat stellen het risico individueel voor U in te schatten. Deze worden opgedeeld in patiënt gebonden risicofactoren, myeloom gebonden risicofactoren en risicofactoren verbonden aan de behandeling (Tabel 3).
Met patiënt gebonden risicofactoren bedoelt men een aantal risico’s die aan U als patiënt zijn verbonden zoals de aanwezigheid van ernstig overgewicht (obesitas), suikerziekte (diabetes), een voorgeschiedenis van een VTE, het dragen van een (poort)katheter, etc.
Met myeloom gebonden risicofactoren bedoelt men een aantal risico’s die zijn verbonden aan uw myeloom zelf, zoals de onmiddellijke fase na diagnose of bij herval wanneer de ziekte op haar hevigst is.
Risicofactoren verbonden aan behandeling omvatten het gebruik van combinatie-chemotherapieschema’s, thalidomide, lenalidomide, pomalidomide, schema’s met zeer hoge doses corticoïden of schema’s met doxorubicine (bijvoorbeeld het VAD schema).
Tabel 3 : Risicofactoren Veneuze Trombo-embolie in patiënten met Multipel Myeloom
|
Individuele risicofactoren Obesitas ( BMI > = 30 kg/m²) Doorgemaakte VTE Centrale katheter/poortkatheter/pacemaker Onderliggende ziektes - Hartlijden (bypass, coronaire stent, hartfalen) - Chronische nierinsufficiëntie - Diabetes mellitus (suikerziekte) - Immobilisatie Heelkunde - Algemene operaties - Anesthesie - Trauma (vb. verkeersongeval) Medicatie - EPO Bloedstollingsziektes
|
Myeloom-risicofactoren Diagnose Hyperviscositeit
Myeloom-behandeling Behandeling met combinatiechemotherapie Gebruik van hoge dosis Gebruik van doxorubicine Gebruik van thalidomide, lenalidomide, pomalidomide
|
Op basis van de hierboven beschreven risicofactoren kan U ingedeeld worden in enerzijds een laag of hoog risicopatiënt en op adequate manier een preventieve behandeling krijgen.
Laag-risicopatiënten worden gedefinieerd als patiënten met géén of maximum één patiënt- of myeloom-gebonden risicofactor. Deze patiënten worden behandeld met een lage dosis aspirine (zoals Asaflow® 80 mg per dag).
Hoog-risicopatiënten zijn alle andere patiënten en worden behandeld met hetzij een dagelijkse onderhuidse injectie van een laag moleculair gewichtsheparine (zoals Clexane® of Fraxiparine®) of met een behandeling met een coumarine-derivaat (Sintrom®, Marevan® of Marcoumar®). Deze laatste zijn pilletjes. Hoewel op het eerste gezicht de coumarine derivaten minder belastend lijken voor de patiënt (pilletjes in tegenstelling tot de dagelijkse spuitjes) bestaat er een nauwe grens tussen een therapeutische dosering en over- of onderdosering. Overdosering kan leiden tot ernstige bloedingen en onderdosering beschermt de patiënt niet tegen VTE. Bovendien kan inname van andere geneesmiddelen en het eten van bijvoorbeeld broccoli of groene groentes interfereren met de spiegels van deze medicatie.
Ondermeer door overwoekering van het beenmerg kan het myeloom een daling van het aantal rode bloedcellen veroorzaken.
Deze vermindering van het aantal rode bloedcellen (bloedarmoede of anemie) wordt in het bloed gemeten aan de hand van het hemoglobinegehalte of het hematocriet.
De symptomen kunnen bestaan uit tekort aan energie, vermeoidheid, benauwdheid of kortademigheid bij inspanning.
Vermoeidheid is een vaak voorkomende klacht van patiënten.
Vermeoidheid wordt veroorzaakt door verschillende factoren en vereist afhankelijk van de herkomst van dit neveneffect een behandeling op maat.
De anemie kan veroorzaakt zijn door de ziekte zelf of door geneesmiddelen die gebruikt worden om kwaadaardige cellen uit te roeien.
Als behandelingsmogelijkheden hebt u:
Erythropoëtine is een natuurlijke "groeifactor" die aangemaakt wordt door de nieren en die het beenmerg aanzet om meer rode bloedcellen aan te maken. Dankzij de stijging van het hemoglobinegehalte vermindert erythropoëtine de moeheid en de noodzaak voor een transfusie.
Botafbraak is een mogelijk gevolg van de ziekte bij multipel myeloompatiënten.
Normaal is er een evenwicht tussen de cellen die bot aanmaken (osteoblasten) en die bot afbreken (osteoclasten).
Bij multipel myeloom is er meer botafbraak dan botaanmaak.
Deze onevenwichtigheid leidt tot botontkalking (vergelijkbaar met osteoperose) alsook tot botafbraak (osteolytische lesies).
Botbreuken met hevige pijn ten gevolge van het broos worden van de botstructuur behoren tot de vervelendste neveneffecten van multipel myeloom.
Radiotherapie kan gebruikt worden om tumorcellen te vernietigen die acute botpijn of beenmergcompressie veroorzaken.
Omdat bij myeloom de ziekte overal verspreid is over het beenmerg, kan radiotherapie niet aangewend worden als basisbehandeling.
Bisfosfonaten zijn moleculen die zich kunnen binden aan de aangetaste botten van myeloompatiënten. Deze binding remt de botafbraak en draagt zo bij aan de genezing en aan het botherstel. Er zijn meerdere types bisfosfonaten, waarvan sommige oraal en andere intraveneus worden toegediend.
Met deze geneesmiddelen kunnen botbreuken echter niet blijvend voorkomen worden. Hoewel hun werkzaamheid afdoende werd bewezen, kunnen ze op lange termijn ook leiden tot neveneffecten, hoofdzakelijk tot " osteonecrose van de kaak". hierbij wordt het kaakbeen gedeeltelijk vernietigd. Het is dus uiterst belangrijk een tandheelkundig onderzoek uit te voeren bij het begin van de behandeling en de tandarts in te lichten over het verloop van de behandeling met bisfosfonaten.
Bisfosfonaten kunnen in sommige gevallen een afname van de nierfunctie ten gevolge hebben. Om deze reden wordt het bloed getest op de klaring van creatine voordat de bisfosfonaten toegedient worden.
Hoge calciumgehaltes in het bloed kunnen duiden op overmatige botafbraak. De symptomen van hypercalciëmie bestaan uit misselijkheid, braken, constipatie, sufheid, vaker plassen en, in extreme gevallen, verwardheid.
Hypercalciëmie kan ook verantwoordelijk zijn voor een plotse verslechtering van de nierfunctie.
De nierfunctie kan bij myeloom omwille van verschillende redenen aangetast zijn:
Daarom wordt de nierfunctie regelmatig gecontroleerd (door meting van het creatininegehalte in het bloed).
De beste manier om deze nierbeschadiging te voorkomen, is behandeling van het myeloom, waarbij de hoeveelheden M-proteïne zo laag mogelijk gehouden worden. In bepaalde gevallen van ernstige nierbeschadiging kan nierdialyse noodzakelijk zijn.
Het is tevens belangrijk goed te hydrateren een geen NSAIDs (niet steroidale anti-inflammatoire geneesmiddelen zoals ibuprofen (Brufen), naproxen (Apranax), diclofenac (Voltaren) en geen jodiumhoidende contraststoffen (injecties welke toegediend worden voor het uitvoeren van een scan) in te nemen of te laten toedienen.
Lotgenotencontact West-Vlaanderen vrijdag 24 mei 2024
Lees meerSymposium Antwerpen ZAS Cadix - 5 oktober 2024
Lees meerHier online te bekijken in kleur
Lees meerElke gift gelijk aan of groter dan 40 euro aan CMP Vlaanderen kan recht geven op een fiscaal attest.
Lees meerMedewerkers voor CMP Vlaanderen
Lees meer|
Evenementenkalender
Ontdek al onze evenementen in een handig overzicht. De meest actuele evenementen vindt u hiernaast. |
Schrijf je nu in op onze CMP Nieuwsflash en blijf op de hoogte van al onze artikelen
